Fristående fortsättning på LC-kost mot fettlever, en svensk studie i fulltext / 1 och del 2
Mycket text har det blivit, men bilder/grafik ger ytterligare perspektiv. Ett sådant är ”Hur snabbt anpassar vi oss till nya förutsättningar?”
För att underlätta tolkningen av 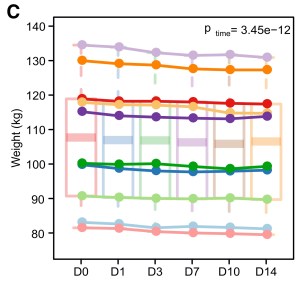 studieresultaten ville man att deltagarna skulle vara viktstabila under de 14 dagar som studien pågick.
studieresultaten ville man att deltagarna skulle vara viktstabila under de 14 dagar som studien pågick.
Det går stick i stäv med hur LCHF normalt fungerar. ”Vi” är vana vid att en väl anpassad LC-kost resulterar i mindre sug, mindre måltider och, om man kan påverka det, längre intervall mellan dem.
Märk väl att fokus initialt bör vara att minska mängden kolhydrater i maten. De som missförstår konceptet och tror att HF är det viktiga och istället ökar mängden fett i maten blir lätt besvikna.
Grundtips: Börja med LC, när hunger eller sug efter mat blir svår att behärska, lägg till lite naturligt animaliskt fett, det är ändå sådant din egen kropp bidrar med när du går ner i vikt.
De pastellfärgade rektanglarna längs ”midjan” i grafen ovan visar den måttliga men tydliga trend man ville motverka, i genomsnitt ungefär -1,8 kg.

Mängden fett i levern påverkades snabbt, redan på tredje dagen är den nedåtgående trenden väl etablerad. Tidsskalan är manipulerad så att nedgången ser mer dramatisk ut än den är.
En lever väger 1,2 – 1,6 kg vilket gör det möjligt att uppskatta hur många gram fett som deltagarna gjorde sig kvitt.
- 1% utgör 12 – 16 gram, 10% 120 – 160 gram och 25% 300 – 400 gram.
Uppskattningsvis minskade fettet 5 – 9% hos de olika deltagarna vilket omräknat i vikt innebär 60/80 – 108/144 gram (den andra siffran i varje par utgår från en 1,6 kg lever). Omräknat till energi kan fettet ha bidragit med 450 – 1300 kcal till fettmetabolismen under dessa 14 dagar. Att gränserna blir så vida beror även på att jag är osäker på om detta fett ska räknas som fettväv med 7500 kcal/kg eller ”rent” fett med 9000 kcal/kg.
I vilket fall framgår tydligt att kroppen metaboliserat som mest 144 gram från leverfett av totala viktnedgången på 1800 gram, som minst 60 gram. Mängden är mycket begränsad, totalt sett, men tas från ett organ som lätt tar skada om det måste långtidslagra fett.
 Levern ”bygger” transportfarkoster, lipoproteiner, med ett inre som passar lipider, t.ex. fett och ett yttre som kan umgås med det vattenhaltiga blodet. I detta fall är det VLDL (very low density lipoprotein) med en ”flagga” på ytan som identifierar dess ursprung i levern, ApoB-100.
Levern ”bygger” transportfarkoster, lipoproteiner, med ett inre som passar lipider, t.ex. fett och ett yttre som kan umgås med det vattenhaltiga blodet. I detta fall är det VLDL (very low density lipoprotein) med en ”flagga” på ytan som identifierar dess ursprung i levern, ApoB-100.
När VLDL är färdigpackat med fettrikt innehåll hamnar det i blodomloppet där kroppens celler får tillfälle att haka fast och plocka det de behöver ur innehållet.
VLDL töms gradvis, krymper och får andra namn, först IDL (intermediate density lipoprotein), därefter LDL (low density lipoprotein) som de riktigt specialiserade delar upp i undergrupper, 5 tror jag det är. Gemensamt för alla är att de har ApoB-100 med sig.
I grafiken står det VLDL-TG vilket verkar lite förvirrande, men när man mäter blodets innehåll av VLDL efter nattfasta kallas det triglycerider, TG. Skillnaden mellan de två är, som jag uppfattar det, att TG förutsätter åtminstone så lång fasta att matens direkta bidrag till fett i blodet är försumbart och levern därför är källan.
”Hur går det ihop att leverfettet minskar trots att koncentrationen VLDL-TG går ner?”
 Det förefaller paradoxalt, men har en helt logisk förklaring.
Det förefaller paradoxalt, men har en helt logisk förklaring.
Beta-hydroxybutyrat, BHB, är en nedbrytningsprodukt som bildas under fettmetabolismen. Det påminner starkt om en kortkedjig fettsyra med 5 kol, smörsyra, men har en väteatom utbytt mot en OH-grupp. Tillsammans med den OH-grupp som kännetecknar alla fettsyror får BHB mycket god förmåga att på egen hand följa blodet utan hjälp av lipoproteiner eller albumin. BHB når utan åthävor kroppens alla hörn och har mycket hög verkningsgrad då den bara innehåller två syre, de övriga atomerna är ännu inte oxiderade och står till mitokondriernas fulla förfogande.
Första dagen ligger BHB ganska tajt runt cirka 0,6 för att redan dag 3 hamna på snett under 2, en ökning med cirka 3 gånger. Detta är ett kvitto på att fettmetabolismen i allmänhet, inklusive den från levern, stiger tydligt. De individuella skillnaderna är stora.
Grafen visar att kroppen metaboliserar fett långt effektivare vid LC och på så sätt ”dränerar” blodet på VLDL-TG vilket förklarar att det halveras redan efter 3 dagar.

DNL (de novo lipogenesis, nybildning av fett i levern) minskar dessutom från dryga 200 till mindre än 100 redan dag 3 för att minska ytterligare något.
I och med LC-kosten minskar pressen på levern att hantera stora mängder glukos i blodet, blodsocker. I vanliga fall sker det genom direkt inlagring i leverglykogen, därefter som niofalt kompaktare fett.
Äter man ”som man borde” är denna fettinlagring i levern helt OK, den är tillfällig och förbrukas när levern exporterar via TG. Problem uppstår när måltiderna blir stora och kommer tätt, då uppstår ingen naturlig efterfrågan på leverfettet och det blir kvar, långt efter sista förbrukningsdatum.
Man studerade även bakteriefloran i tjocktarmen och fann:
Among the top ten most abundant of 25 significantly altered genera, only Streptococcus, Lactococcus, and Eggerthella were increased over the study period (Figure 2C; Table S2). The carbohydratedegrading bacteria Ruminoccocus, Eubacterium, Clostridium, and Bifidobacterium were all decreased (Figure 2C; Table S2). In parallel, we observed decreased carbohydrate fermentation as shown by reductions in fecal concentrations of short-chain fatty acids (SCFAs) (Figure 2D), in agreement with previous studies (David et al., 2014; Duncan et al., 2007).
Min tolkning: Bland de 10 mest förekommande bakterierna (av 25 statistiskt säkerställt förändrade) var det endast tre typer av bakterier som ökade under studieperioden. Fyra bakterier som bryter ner kolhydrater minskade i antal. Vi observerade även en minskning i mängden av kolhydratnedbrytning då koncentrationen av kortkedjiga fettsyror (SCFA) minskade.
Sammanlagt minskade 7 av 10 i topp vanligaste bakterierna varav logiskt nog 4 var direkt engagerade i nedbrytning av kolhydrater, det studiens deltagare drastiskt minskade. Ökningen av SCFA var ett annat, parallellt, tecken på detta. De räknas som fördelaktiga för tjocktarmens drift och hälsa, hämmar till och med coloncancer. Fibrer är den sannolikt viktigaste energikällan för de kolhydratdrivna bakterierna då de tillhör de få kolhydrater som i större mängd lyckas ta sig förbi tunntarmen. Våra kroppar är ekonomiska och anpassar sig genom att minska på det som inte behövs, en aspekt av homeostasen.





