Fristående fortsättning från LC-kost mot fettlever, en svensk studie i fulltext / 1
In hyperinsulinemic subjects with NAFLD, hepatic DNL accounts for approximately 25% of liver triglyceride content (Diraison et al., 2003; Donnelly et al., 2005); thus, carbohydrate restriction, combined with exercise and regular follow-up, has emerged as an effective dietary intervention for obesity (Astrup et al., 2004; Foster et al., 2003) and NAFLD (Rinella and Sanyal, 2016).
Min tolkning: Hos personer med förhöjt insulin och NAFLD (icke alkoholberoende fettlever) står DNL (de novo lipogenesis, nyproduktion av fett) för 25% av leverns innehåll av triglycerider (fett). Reduktion av kolhydrater i maten i kombination med fysisk aktivitet och regelbunden uppföljning har visat sig vara effektivt mot övervikt/fetma.
Källa: Fulltexten av http://www.cell.com/cell-metabolism/fulltext/S1550-4131(18)30054-8
Avsikten var att fokusera på LC-kostens inverkan på leverns fettförråd, av det skälet ville man motverka ”allmän viktnedgång” för att inte behöva hantera så många samvarierande parametrar.
To investigate how liver fat metabolism is affected by reduced carbohydrate consumption without a concomitant reduction in calorie intake, we served a pre-prepared isocaloric low-carbohydrate diet with increased protein content (<30 g of carbohydrates and an average of 3,115 kcal per day)
Min tolkning: För att undersöka hur leverns fettmetabolism påverkas av en reducerad kolhydratkonsumtion utan samtidig minskning av energitillförseln serverade vi förberedda LC-måltider med ökat proteininnehåll, <30 g kolhydrater och ett genomsnitt på 3,115 kcal per dag.
De 10 deltagarna var i olika grad obesa, vikten varierade mellan cirka 80 – 140 kg. Energibehovet beror i stor utsträckning av kroppens yta snarare än dess vikt, av det skälet känns uppgiften om det genomsnittliga energiintaget lite meningslös. Dessutom var deltagarna antingen tydligt eller ordentligt över eller under ”medelvikten”, ingen ”på” den.
To minimize the weight loss that is known to occur on a short-term isocaloric carbohydrate-restricted diet (Kekwick and Pawan, 1956), the study subjects were in daily contact with a dietician and were instructed to increase their daily energy intake whenever their weight decreased between two study days by more than 0.2 kg.
Min tolkning: För att motverka (naturlig) viktminskning till följd av LC-kost stod deltagarna i daglig kontakt med en dietist och var instruerade att öka energiintaget om vikten minskade mer än 0,2 kg från en dag till annan.
Notera: Kekwick och Pawans studie från 1956 är en klassiker i LCHF-sammanhang.
In contrast to the small reduction in weight loss, we observed dramatic reductions in liver fat, as measured by magnetic resonance spectroscopy (MRS), in all the individuals over the 14-day study period (mean reduction 43.8%; Figure 1E). Of note, the reduction was significant just 1 day after the start of the diet intervention (p = 0.027) and was paralleled by a significant decrease in total liver volume (Figure S1).
Min tolkning: I kontrast till den lilla förändringen i kroppsvikt observerade vi dramatiska minskningar i leverfettet hos alla deltagare över studieperioden. Minskningen var i medeltal 43,8%*. Notabelt är att minskningen var statistiskt säkerställd redan efter 1 dag.
Med så dramatiska förbättringar och tydliga skillnader redan inom ett dygn är det anmärkningsvärt att vården ”missat” att utnyttja denna enkla strategi för att motverka NAFLD!
We observed marked reductions in very-low-density lipoprotein (VLDL)-triglycerides (mean reduction 56.7%; Figure 1F) and in fasting plasma triglyceride concentrations (mean reduction 48.4%; Table S1) at the end of the study.
Min tolkning: Vi observerade tydliga sänkningar av VLDL (minskning i medeltal 56,7%), vid studiens slut och efter fasta sjönk värdet, nu kallat TG, i medeltal med 48,4%.
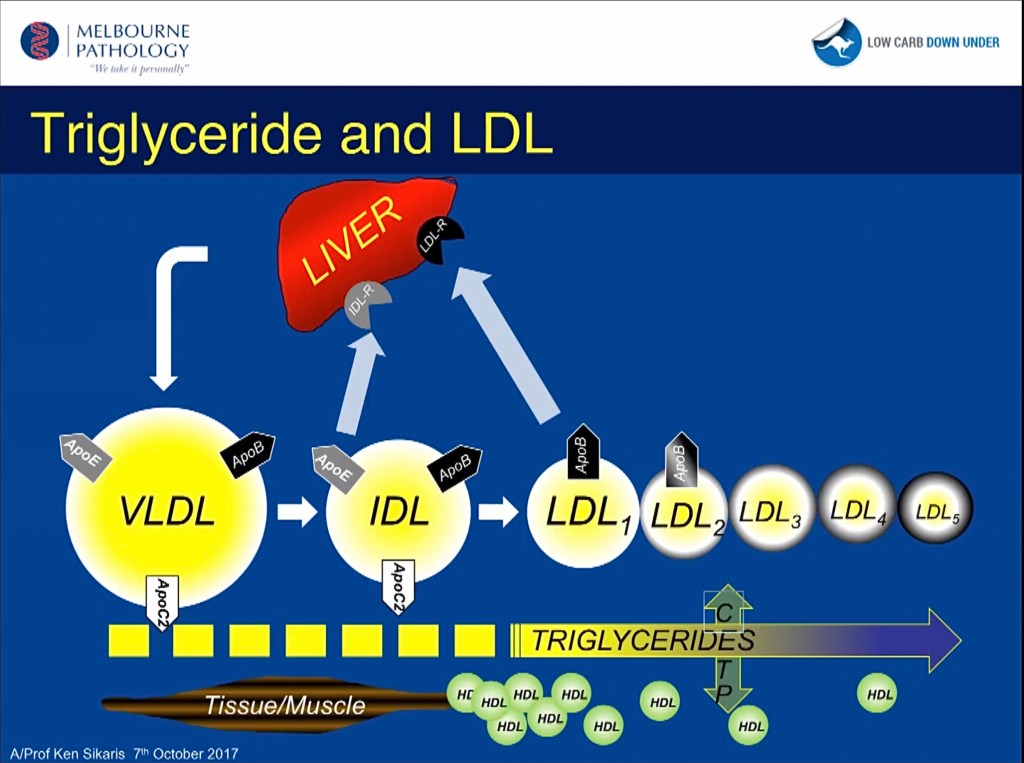
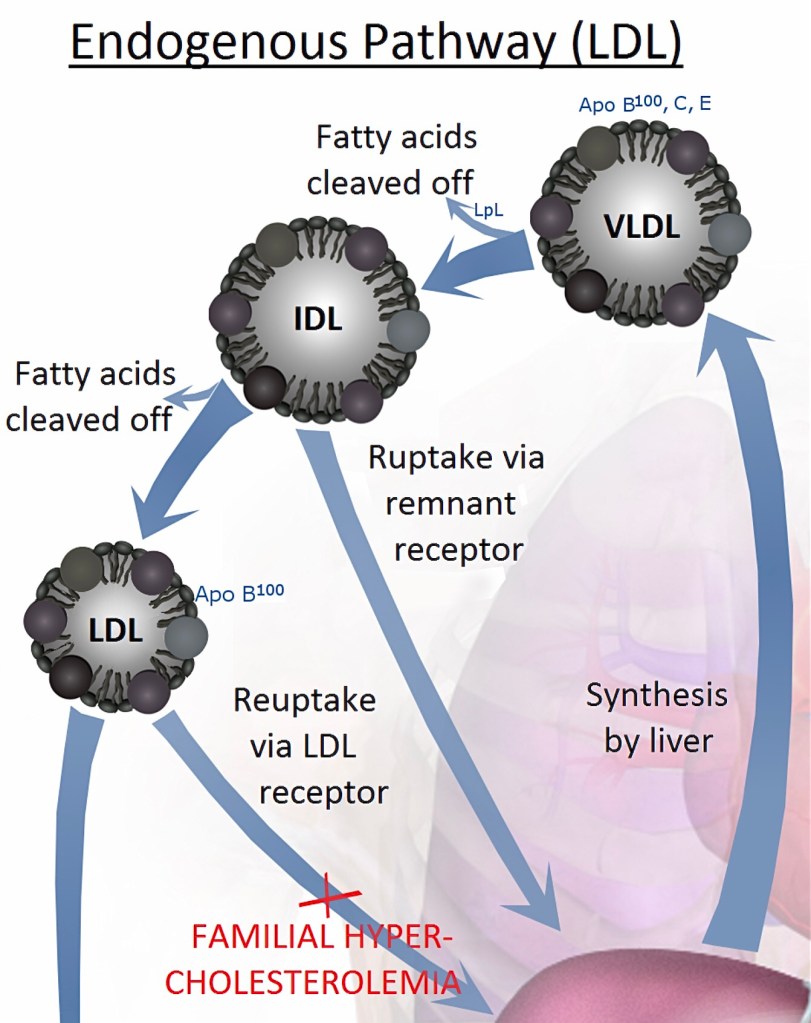
VLDL (very low density lipoprotein) är en transportfarkost för lipider (fetter och fettliknande ämnen) som bildas i levern med ApoB-100 som ID. I föregående inlägg nämnde jag den närbesläktade ApoB-48, unik för chylomikronen som transporterar främst de långkedjiga fetterna direkt från maten ut till de kroppsceller som har omgående behov av dem, till fettväv för lagring samt slutligen levern där chylomikronen slutligen plockas isär och återvinns med den fettslatt som återstår.
Med hjälp av dessa två ApoB-varianter går det att skilja på ursprunget för fetter, ApoB-48 om det kommer direkt från maten, ApoB-100 om det varit en vända i levern eller producerats där. VLDL efter nattfasta när matens direkta bidrag är slut anger leverns export ur egna lager samt DNL (de novo lipogenesis = egen nyproduktion av fett)
In addition, we found a significant reduction of plasma apolipoprotein C-III (apoC-III) (Figure 1G), an inhibitor of VLDL clearance (Ginsberg et al., 1986) and a strong correlation between decreases in the concentration of apoC-III and VLDL-triglycerides over the study period (r = 0.91, p = 0.0015; Figure S2).
Min tolkning: Vi noterade en statistiskt säkerställd reduktion av ApoC-III som hämmar två enzymer, lipoprotein lipase samt hepatic lipase vilka båda behövs för att ”tömma VLDL”. Det fanns en stark samvariation mellan ApoC-III och VLDL under studietiden.
Följande är goda skäl att leverfettet består av lokalproducerat fett med kolhydrater som råvara.
We also analyzed the composition of VLDL-triglycerides and observed a decreased proportion of saturated fatty acids including myristic acid (14:0) and palmitic acid (16:0) and an increased proportion of unsaturated fatty acids such as oleic acid (18:1) (Table S1).
Min tolkning: Vi analyserade sammansättningen av fettet i VLDL och noterade en minskning av mättad myristinsyra (14:0) och palmitinsyra (16:0) (14 resp. 16 anger antal kol i kolkedjan medan 0 anger antal dubbelbindningar) samt en ökad andel enkelomättade fettsyror som oljesyra (18:1).
När kroppen själv bygger fettsyror från grunden sker det fram till 16 kol i kedjan och inga dubbelbindningar, palmitinsyra. Den kan därefter bearbetas av två enzymer, ett elongas som lägger till ett extra kol med två tillhörande väte, samt ett desaturas som kan skapa en dubbelbindning i kolkedjan genom att plocka bort väteatomer, en från vardera av två intilliggande kolatomer. De bindningar som då frigörs hakar genast i varandra och blir en dubbelbindning, en omättnad. Den tidigare raka men relativt flexibla kolkedjan kröker sig i dubbelbindningen. Fetter som byggs enbart av mättade fetter blir ”stelare” ju längre kolkedjan är då de packas tätare till varandra. Trots att oljesyran är snäppet längre kommer omättnaden och krökningen att den blir flytande.
To test whether the marked reductions in liver fat were linked to the diet intervention, we performed a follow-up MRS in seven of the ten participants 1–3 months after completing the intervention study and returning to their normal diet. We observed that their liver fat content returned to a level similar to that measured before the diet intervention (11.3% ± 1.6% at follow-up versus 13.8% ± 2.5% at baseline, p = 0.08).
Min tolkning: För att kontrollera om de tydliga minskningarna i leverfett berodde på LC-kosten följde vi upp med en MRS på 7 av 10 deltagare efter 1 – 3 månader, när de återfallit i gamla matvanor. Vi fann att deras levrar var förfettade i jämförbar nivå med den innan studien (11.3% ± 1.6% mot initialt 13.8% ± 2.5%).
Att delta i denna studie för att avfetta levern har lärt deltagarna nada, zilch!
*) I sammanhang som dessa är det legio att presentera mätresultat och statistiska finurligheter med en anmärkningsvärt hög precision, i detta fall att fettandelen i levern minskade 43,8%.
Sällan eller snarare aldrig redovisas de oundvikliga fel som mätmetoder av tekniska skäl aldrig kan undvika, inte heller den tillkommande felkälla som mer eller mindre erfarna operatörer gör sig skyldiga till. I ”hårda vetenskaper” som t.ex. fysik är det absolut krav att mätningar och resultat av dem presenteras inklusive alla de fel som inte kan undvikas.
I ”mjuka sammanhang” tycks man systematiskt undvika allt sådant och den variation man redovisar är de som beror på att ”alla människor är olika”. Vetenskaplig mognad, att i första rummet sortera bort felaktiga hugskott och hypoteser, är måttligt utbredd om den alls förekommer. Här är målet snarare att stödja en hypotes även om den statistiska signifikansen är så mesig som 1/20, detta utan att ha tagit hänsyn till de tillkommande fel som beror av mätmetoder och mänskliga fel.
Märk väl att kritiken gäller generellt, denna studie är inte ”värre” än andra.