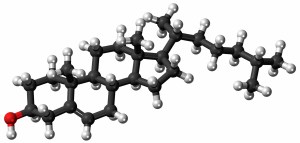
Kolesterol är en molekyl med 4 sammankopplade kolringar, med en OH-ände samt en kolkedja på motsatt sida. 
OH-änden (det står HO i bilden) är viktig, den ger kolesterolet orientering i sin omgivning och en punkt där andra molekyler kan ”haka på”, förestra. När det sitter som en stabilisator i ett alltför sladdrigt cellmembran (för många omättnadspunkter i de ingående fettsyrorna) kommer OH-änden att vändas mot cellmembranets yta och andra änden med sina lipofila (”fettälskande”) metylgrupper (de som slutar i CH3/H3C) hamnar inne bland fettsyrorna. Kolesterol är även råmaterial för D-vitamin, steroidhormoner samt fungerar som isolator runt nervtrådar så att dess svaga elektriska signaler inte skingras eller störs utifrån. Det senare kan vara relevant i studien jag tar upp idag.

Denna livsviktiga molekyl har helt oförskyllt fått ge sitt namn till ett antal lipoproteiner*, transportfarkoster, som fraktar runt ämnen som inte på egen hand kan transporteras i blodomloppet, detta då de inte är lösliga i blod och inte ”vet” vart de ska. I vilket fall har medicinindustrin gett sig på produktionen av kolesterol med en grupp kemikalier som kallas statiner. Tidigt i kroppens syntes av kolesterol blockerar dessa en stor del av produktionen inklusive en mängd andra ämnen som ligger ”nedströms” detta ställe.
Statiner är medicinindustrins verkliga kassapjäs, de drar in otaliga miljarder per år utan att de för den skull har en nettofördel för hälsa och överlevnad. Mer om detta finns att läsa på Internet.
Under de allra senaste åren har de röster som ifrågasätter den närmast hämningslösa förskrivningen av statiner, dels på grund av deras bleka verkan men mest på grund av deras negativa ingrepp i hälsan, i detta fall minnesförlust. Självklart sitter inte industrin still i båten när ekonomin naggas i kanten, de försöker med olika medel visa sina produkters förträfflighet eller åtminstone att de inte skadar. Så mycket. Men ibland skiner desperation och dumhet igenom så uppenbart att det kunde ha skrivits av Galenskaparna.
Ett exempel är Statin Therapy and Risk of Acute Memory Impairment där försteförfattaren är Brian L. Strom**
Importance Reports on the association between statins and memory impairment are inconsistent.
Min tolkning: Rapporter om samband mellan statiner och minnesförsämring är förvirrande.
Fladdriga data och flimsiga slutsatser förekommer ofta i kost-, medicin- och andra ”mjuka” områden där den vetenskapliga metoden inte mognat till ingenjörs– och fysikernivå.
Objective To assess whether statin users show acute decline in memory compared with nonusers and with users of nonstatin lipid-lowering drugs (LLDs).
Min tolkning: Vi önskar fastställa om statinanvändare visar försämring av minnet jämfört med ickeanvändare och de som behandlas med lipidsänkare andra än statiner (nsLLD).
Inget att anmärka på så långt, en statingrupp, en kontrollgrupp samt en nsLLD-grupp.
Design, Setting, and Participants Using The Health Improvement Network database during January 13, 1987, through December 16, 2013, a retrospective cohort study compared 482 543 statin users with 2 control groups: 482 543 matched nonusers of any LLDs and all 26 484 users of nonstatin LLDs. A case-crossover study of 68 028 patients with incident acute memory loss evaluated exposure to statins during the period immediately before the outcome vs 3 earlier periods. Analysis was conducted from July 7, 2013, through January 15, 2015.
Min tolkning: Man använde data från The Health Improvement Network database från den 13/1 1987 till 16/12 2013, en retrospektiv (”tillbakatittande”) studie där man jämförde 482 543 statinanvändare med 2 kontrollgrupper: 482 543 matchade kontroller samt 26 484 nsLLD-användare.
En uppenbar glidning från den vetenskapliga metoden, plötsligt finns där 2 kontrollgrupper, en obehandlad (helt som det ska vara) och en med alternativ behandling.
Results When compared with matched nonusers of any LLDs (using odds ratio [95% CI]), a strong association was present between first exposure to statins and incident acute memory loss diagnosed within 30 days immediately following exposure (fully adjusted, 4.40; 3.01-6.41). This association was not reproduced in the comparison of statins vs nonstatin LLDs (fully adjusted, 1.03; 0.63-1.66) but was also present when comparing nonstatin LLDs with matched nonuser controls (adjusted, 3.60; 1.34-9.70). The case-crossover analysis showed little association.
Min tolkning: Efter 30 dagars medicinering fanns ett starkt samband mellan statiner och minnesförlust, 4,4 gånger högre jämfört med ickebehandlade. Detta samband fanns inte när man jämförde statinanvändare med LLD-användare, skillnaden var där 3%. Vid jämförelse mellan LLD-behandlade och ickeanvändare var minnesförlusten 3,6 gånger till LLD-behandlades nackdel.
Nu är det dags att reflektera lite över vad, och hur, man skriver. I mittenmeningen hävdar man att statinanvändare inte får sämre minne än de som behandlas med LLD och det låter ju positivt, 3% skillnad är knappt värt att nämna. Detta sätt att presentera data tar lite udden av att båda behandlingsgrupperna hade kraftigt försämrat minne jämfört med de obehandlade. Utan att ha läst fulltexten kan jag inte förstå betydelsen av sista meningen, ”The case-crossover analysis showed little association.” Min misstänksamma sida tänker att ”…visade svagt/inget samband…” är där för att förvirra läsaren.
Conclusions and Relevance Both statin and nonstatin LLDs were strongly associated with acute memory loss in the first 30 days following exposure in users compared with nonusers but not when compared with each other. Thus, either all LLDs cause acute memory loss regardless of drug class or the association is the result of detection bias rather than a causal association.
Min tolkning: Både statin- och LLD-användare visade starkt försämrat minne efter 30 dagars användning jämfört med ickeanvändare men inte sinsemellan. Antingen förorsakar alla lipidsänkare minnesförsämringar eller så beror effekten på att användarna lättare upptäcker sin minnesförlust snarare än att det finns ett orsakssamband.
Men jösses, läs det där sista igen, helst den engelska texten. Dom antyder att de som äter kolesterolsänkande medel är bättre på att upptäcka att deras minne försämrats 3,6 till 4,4 gånger!
Lite off topic men ändå relevant: 97% of drug trials back the firm that paid for them.
Så till en artikel där försteförfattaren Brian L. Strom intervjuas under rubriken Study Questions Statin, Memory Loss Connection. Innan du klickar in på den så tänk efter om rubriken matchar innehållet i abstractet ovan.
Strom noted that without the non-statin LLD control group in his study, the findings would have shown a strong association between statin initiation and short-term memory loss.
”In the absence of this control group, the finding would have been completely misleading,” he said.
Min tolkning: Strom menar att utan nsLLD-gruppen i studien kunde slutsatsen ha blivit att statinanvändning leder till minnesförlust. ”I avsaknad av denna kontrollgrupp kunde slutsatsen ha blivit fullständigt missvisande.”
Ser du det fullkomligt absurda i denna slutsats?
Strom said the study findings should reassure both patients and physicians who prescribe statins.
Min tolkning: Strom sade att studiens resultat bör lugna både patienter och läkare som förskriver statiner.
Albert Einstein lär ha sagt att såväl Universum som mänsklig dumhet är oändliga men att han var lite osäker om Universum.
Tom Naughton har skrivit mycket bildlikt och roande om detta
*) De vanligaste omtalade är små täta LDL som har sitt ursprung i kolhydratkonsumtion, stora fluffiga LDL som gynnas av fet mat och HDL som anses städa upp i blodomloppet. Du har hört dem kallas ”ont kolesterol” och ”gott kolesterol”. Bullshit, allt kolesterol är lika, dessutom livsavgörande. Sista L-et i varje sådan bokstavskombination står för lipoprotein, alltså att det är en transportfarkost.
**) The research was funded by the National Institutes of Health. Strom reported receiving research funding from AstraZeneca and Bristol-Myers Squibb and serving as a consultant to Abbott, AstraZeneca, Bayer Healthcare, Bristol-Myers Squibb, Novartis and Pfizer. A co-author reported receiving research funding from AstraZeneca and Bristol-Myers Squibb and serving as a consultant to AstraZeneca, Bayer Healthcare, Bristol-Myers Squibb, and Merck.