Den 17 november 2005 började både jag och min fru Iva äta enligt lågkolhydratprinciper efter att ha sträckläst Fettskrämd av Lars-Erik Litsfeldt samt Ät dig ner i vikt av Sten Sture Skaldeman.
Snart nog började media att kommentera detta fenomen som gick mothårs allt heligt bland näringspurister. Tidningsartiklar om LCHF avslutades försiktigtvis med faktarutor av typen ”Hjärnan behöver socker!”, ”Fett är farligt!” och ”De som äter såhär förkortar sina liv!”.
En uthållig bastion för socker och mot fett i maten var Livsmedelsverket. De slingrade sig när studier inte visade negativa följder av LCHF, snarare tvärtom. Till slut valde man att ”…en samlad bedömning…” skulle ingå i deras argumentering. Ur vetenskaplig synvinkel är det undermåligt, beviskedjan måste hänga samman, inte bara bestå av många länkar.
Nåja, idag, 17 år senare får jag ett nyhetsbrev från Livsmedelsverket
Tillsatt socker och sockersötade drycker ökar risken för bland annat fetma, typ 2-diabetes och karies. Ju mer tillsatt socker, desto större risk. Det är den slutliga bedömningen i en vetenskaplig genomgång från den europeiska livsmedelssäkerhetsmyndigheten Efsa.
https://www.livsmedelsverket.se/om-oss/press/nyheter/pressmeddelanden/tydligt-samband-mellan-tillsatt-socker-och-ohalsa
Efter en genomgång av över 30 000 publikationer över hälsoeffekter av socker samt synpunkter från remissinstanser har Efsa fastställt sin bedömning.
– Efsas genomgång visar att det, precis som vi sett tidigare, finns ett tydligt samband mellan tillsatt socker och bland annat fetma, typ 2-diabetes, höga blodfetter och högt blodtryck. De vetenskapligt säkraste sambanden ses för läsk, säger Anna Karin Lindroos, nutritionist på Livsmedelsverket.
”…precis som vi sett tidigare…”. Jo tjenare, LCHF-are spådde tidigt att när Livsmedelsverket och andra tröga till slut tvingas ändra hela eller delar av sina åsikter så skullen just den meningen ingå.
Viktigt att begränsa konsumtionen av socker
Genomgången har gjorts efter önskemål från Sverige och de övriga nordiska länderna. Ett av önskemålen var att Efsa skulle ta fram en övre gräns för hur mycket tillsatt socker man kan äta innan det blir ohälsosamt.
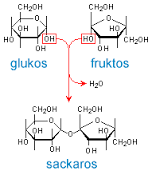
Tillsatt socker är ett lurigt begrepp. Då marknaden (konsumenter) vants med söt smak är det inte självklart att minska sockret. Ett sätt att slingra sig är att tillsätta koncentrerad juice, en annan att använda HFCS, en produkt där man ökat andelen fruktos [1] som bidrar med sötma. Många andra varianter finns.
Efsas slutsats är att risken för skadliga effekter på hälsan ökar linjärt, det vill säga ju mer tillsatt socker man äter desto mer ökar risken för ohälsa. Mot bakgrund av det bedömer Efsa att det inte går att sätta en övre gräns för hur mycket tillsatt socker man kan äta utan risk för negativa hälsoeffekter, utan att konsumtionen bör vara så låg som möjligt.
Efsa sätter ingen övre gräns där hälsan på ett eller annat sätt påverkas negativt, konsumtionen ska vara så låg som möjligt.
–Det är en gedigen vetenskaplig genomgång som Efsa har gjort och som vi kommer att använda när vi uppdaterar våra råd. Men även ett viktigt underlag för andra insatser som görs för att minska sockerkonsumtionen i Sverige, säger Anna Karin Lindroos.

De nordiska näringsrekommendationerna revideras för närvarande och Livsmedelsverket deltar tillsammans med forskare och myndigheter i de andra nordiska länderna.
Added and free sugars should be as low as possible – Efsa
Socker – Livsmedelsverket
[1] Fruktos är den monosackarid som ger söt smak. Fruktosen har ingen roll (Jo, det finns en, specifik för män. Fundera och ta reda på, anternativt fråga i en kommentar) i kroppens näringsbehov förrän den byggts om av levern till leverglykogen eller fett. Det senare kan lagras i levern och ger fettlever! En gång i tiden var fettlever ett säkert tecken på alkoholism, så är det inte längre. Nu kan det vara NAFLD, Non Alcoholic Fatty Liver Disease.